द्रव्य के तापीय गुण एवं ऊष्मागतिकी
Category :
द्रव्य के तापीय गुण एवं ऊष्णागतिकी
विश्लेषणात्मक अवधारणा
ठोसों के विपरीत तरल की अपनी कोई निश्चित आकृति नहीं होती है। ठोसों एवं द्रवों का निश्चित आयतन होता है जबकि गैस पात्र के कुल आयतन को भर देती है। ऊष्मा ऊर्जा का एक रूप है जो किसी पिंड तथा उसके परिवर्ती माध्यम के बीच उनमें तापांतर के कारण प्रवाहित होती है। किसी पिंड तप्तता की कोटि मात्रात्मक रूप में ताप द्वारा निरूपित होती है। ऊष्मागतिकी के द्वारा निकायों की ऊष्मा व ऊर्जा का अध्ययन तथा सभी पदार्थों में अणु की गतियों से सम्बन्धित अध्ययन करेगे।
ऊष्मा
ऊष्मा, ऊर्जा का ही एक रूप है जिसके द्वारा किसी वस्तु की गर्माहट अथवा ठंडक का अनुभव होता है। जब एक गर्म वस्तु तथा एक ठंडी वस्तु को परस्पर संपर्क में लाया जाता है। इस प्रक्रिया में स्थानांतरित ऊर्जा ही ऊष्मा है। प्रत्येक पदार्थ के अणुओं की अनियमित गति के कारण पदार्थ की ऊर्जा को ही ऊष्मीय ऊर्जा कहते है।
एक ग्राम पानी का ताप \[14.5{}^\circ C\] से \[15.5{}^\circ C\] तक बढ़ाने के लिए आवश्यक ऊष्मीय ऊर्जा का मान एक कैलोरी के तुल्य होता है। ऊष्मीय ऊर्जा का SI मात्रक- जूल होता है। 1 कैलोरी = 4.186 जूल
ताप का प्रभाव
ताप बढ़ने से पदार्थ का आयतन भी बढ़ता है।
ताप घटने से वायु में ध्वनि का वेग घटता है।
ताप बढ़ने से पदार्थ की अवस्था भी परिवर्तित हो सकती है।
तापमापी का सिद्धांत (Principle of Thermometer)
तापमापी बनाते समय निम्न बातों का ध्यान रखना पड़ता है। (i) तापमापी के पदार्थ का चयन (ii) तापमापी का आंशकन (iii) तापमापी की सुग्राहिता
तापीय प्रसार गुणांक- अधिकांश पदार्थों में ताप वृद्धि से उनके आकार में वृद्धि होती है। इसे ही ऊष्मीय या तापीय प्रसार कहते है। (i) रेखीय प्रसार गुणांक, (ii) क्षेत्रीय प्रसार गुणांक एवं (iii) आयतन प्रसार गुणांक।
ये तीन प्रकार का प्रसार ताप मान में वृद्धि होने के कारण होता है। गैसों के लिए आयतन प्रसार गुणांक का मान ताप पर निर्भर करता है तथा ताप में वृद्धि के साथ कम हो जाता है।
परम ताप- किसी भी पदार्थ का न्यू नतम ताप परम ताप या शून्य ताप कहलाता है।
विशिष्ट ऊष्मा- किसी पदार्थ के एकांक द्रव्यमान के ताप में एकांक ताप की वृद्धि करने के लिए आवश्यक ऊष्मा की मात्रा को उस पदार्थ की विशिष्ट ऊष्मा कहा जाता है। मात्रक- कैलोरी/कि.ग्रा. \[{}^\circ C\] होता है। SI मात्रक- जूल/कि.ग्रा. \[{}^\circ C\] होता है। जल की विशिष्ट ऊष्मा सर्वाधिक होती है। गैसों में हाइड्रोजन की विशिष्ट ऊष्मा अधिक होती है।
विशिष्ट ऊष्माधारिता- किसी पदार्थ के एकांक द्रव्यमान का ताप 1 K या \[1{}^\circ C\] बढ़ाने के लिए आवश्यक ऊष्मा की मात्रा को उस पदार्थ की विशिष्ट ऊष्माधारिता कहते है।
\[\]
मात्रक- जूल प्रति कि.ग्रा. केल्विन या कैलोरी प्रति ग्राम \[{}^\circ C\] होता है।
विमीय सूत्र- \[\left[ {{M}^{0}}{{L}^{2}}{{T}^{-2}}{{K}^{-1}} \right]\]
अवस्था परिवर्तन- जब पदार्थ एक भौतिक अवस्था से दूसरी भौतिक अवस्था में परिवर्तन होता है तो इस घटना को अवस्था परिवर्तन कहते है।
जैसे- जल का उबलकर वाष्प में बदलना तथा वाष्प का ठंडा होकर जल में बदलना अवस्था परिवर्तन के उदाहरण हैं।
अवस्था परिवर्तन के दौरान ताप नियत रहता है। दी गई ऊष्मा का उपयोग अवस्था परिवर्तन के काम आता है। जिससे पदार्थ का आन्तरिक ऊर्जा में वृद्धि होती है।
गुप्त ऊष्मा (Latent Heat)- किसी पदार्थ का ताप परिवर्तित किए बिना इसकी अवस्था परिवर्तन के लिए आवश्यक ऊष्मा की मात्रा को पदार्थ की गुप्त ऊष्मा कहते हैं। यदि पदार्थ का द्रव्यमान m तथा अवस्था परिवर्तन के लिए आवश्यक ऊष्मा \[\] जबकि पदार्थ का ताप नियत रहे। जहां L = गुप्त ऊष्मा है।
SI पद्धति में गुप्त ऊष्मा का मात्रक- जूल/कि.ग्रा. है।
विमा- \[[{{M}^{0}}{{L}^{2}}\text{ }{{T}^{-2}}]\]
गुप्त ऊष्मा दो प्रकार की होती है।
(i) गलन (बर्फ) की गुप्त ऊष्मा- 336 जूल।
(ii) वाष्पन की गुप्त ऊष्मा - 2268 किलो-जूल/कि.ग्रा. है।
ऊष्मा का चालक- वे पदार्थ जिनके अंदर से होकर ऊष्मा का संचरण हो सकता है ऊष्मा का चालक कहलाते है।
ऊष्मा का सुचालक- जिन पदार्थों के अंदर से होकर ऊष्मा का संचरण बहुत तीव्रता से होता है। सुचालक कहलाता है। जैसे -तांबा, लोहा, चांदी।
ऊष्मा का कुचालक- ऊष्मा का संचरण बहुत कम होता है। कुचालक कहलाते हैं। जैसे- लकड़ी, कपड़ा, कांच, वायु, ऊन इत्यादि।
ऊष्मारोधी- वे पदार्थ जिनके अंदर से होकर ऊष्मा का चालन बिल्कुल ही नहीं हो पाता वे ऊष्मारोधी कहलाते हैं। जैसे- ऐजबेस्टस, ऐबोनाइट काली और खुरदुरी सतह ऊष्मा की सबसे अच्छी अवशोषक और उत्सर्जक होती है जबकि चमकदार और चिकनी सतह. ऊष्मा की सबसे कम अवशोषक एवं उत्सर्जक होती है।
कृष्णिका या आदर्श कृष्ण पिंड (Perfect Black Body)- कृष्णिका वह वस्तु है जो अपने पृष्ठ पर आपतित संपूर्ण विकिरण को चाहे वह किसी भी तरंग दैर्ध्य का क्यों न हो अवशोषित कर लेता है। अभी तक कोई भी ऐसी वस्तु नहीं खोजी जा सकी है जो आदर्श कृष्णिका हो फिर भी दीप, काजल, चपड़ा (कोलतार), इंडिया इंक तथा प्लेटिनम की कालिख को आदर्श कृष्णिका के समान होता है। कृष्णिका का रंग आवश्यक एक बंद भट्टी को भी लगभग कृष्णिका कहा जाता है। कृष्णिका का रंग आवश्यक रूप से काला होना ही आवश्यक नहीं है।
किरचॉफ के नियम के अनुसार- किसी निश्चित ताप पर किसी दी हुई तरंग दैर्ध्य के लिए प्रेत्यक वस्तु की स्पेक्ट्रमी उत्सर्जन क्षमता तथा स्पेक्ट्रमी अवशोषण क्षमता का अनुपात एक नियतांक होता है। जो उसी तरंग दैर्ध्य के लिए आदर्श कृष्णिका की स्पेक्ट्रमी उत्सर्जन क्षमता के बराबर होती है।
यदि कोई पृष्ठ किसी विशेष तरंग दैर्ध्य के विकिरण का अच्छा अवशोषक होता है तो वह उसी के विकिरण का अच्छा उत्सर्जन भी होगा।
गैस एवं अणुगति सिद्धांत
आदर्श गैसः आदर्श गैस एक ऐसी काल्पनिक गैस है जिसके गुण किसी भी वास्तविक गैस के अत्यन्त निम्न दाब पर गुणों के समान होते हैं। आदर्श गैस में निम्न गुणों की कल्पना की जाती है
इनके आयतन प्रसार गुणांक व दाब प्रसार गुणांक बराबर होते है। इनके अणुओं के मध्य आकर्षण बल नहीं लगता है। इनके अणुओं का आकार अत्यन्त सूक्ष्म होता है। ये गैस ताप व दाब की सभी अवस्थाओं में बॉयल, चार्ल्स एवं दाब के नियमों का पूर्णतः पालन करती है। दाब (P), आयतन (V) और परम ताप (T) में संबंध स्थापित करने वाली आदर्श गैस समीकरण है,
\[\]
यहां \[\mu \] गैस में मोलों की संख्या और N अणुओं की संख्या है। R तथा \[{{K}_{B}}\] क्रमशः सार्वत्रिक गैस नियंताक एवं वोल्टजमान नियंताक है।
\[R=8.314\,J.mo{{1}^{-1}}{{K}^{-1}},{{K}_{B}}=\frac{R}{{{N}_{A}}}=1.38\times {{10}^{-23}}\,J.{{K}^{-1}}\]
वास्तविक गैसें, आदर्श गैस समीकरण का अधिकाधिक पालन केवल उच्च ताप तथा निम्न दाब पर ही करती है।
गैसों का गव्यात्मक सिद्धांत (Kinetic Theory of Gases): एक गैस के सभी अणु समान होते हैं। अणु हर संभव वेग से हर संभव दिशा में गतिमान होता है। अणुओं की टक्कर पूर्णतया प्रत्यास्था होती है। गैस के गतिशील अणु जब बर्तन की दीवार से टकरातें है तो उनके संवेग में परिवर्तन होता है, जिसके कारण गैस बर्तन की दीवारों पर दबाव उत्पन्न करती है।
गैसों के अणुगति सिद्धांतो की परिकल्पना- गैसों के विभिन्न भौतिक गुणों की गैसों के अणुगति सिद्धांत से व्याख्या करने के लिए। निम्न परिकल्पनाएं ली जाती है:
(i) एक गैस के सभी अणु आकार तथा द्रव्यमान में समान और पूर्णतः प्रत्यास्थ होते है। (ii) गैस के अणुओं का आयतन गैस के आयतन की तुलना में नगण्य होता है। (iii) गैस के अणुओं का वेग \[\left( 0,\infty \right)\] के बीच होता है तथा वे हर संभव वेग से हर संभव दिशा में गतिमान होते हैं। (iv) गैस के अणुओं के बीच टक्कर पूर्णतया प्रत्यास्था होती है तथा अणुओं की टक्कर में लगा समय नगण्य होता है। (v) अणुओं के बीच कोई आकर्षण तथा प्रतिकर्षण बल कार्य नहीं करता है। (vi) गैस के अणुओं पर गुरुत्वाकर्षण बल प्रभावी नहीं होता है क्योंकि अणुओं का द्रव्यमान सूक्ष्म तथा वेग अधिक होता है। (vii) गैस का घनत्व पूरी गैस के सभी भागों में लगभग समान होता है।
ऊष्मागतिकी (Thermodynamics)
ऊष्मागतिकी- भौतिक विज्ञान की वह शाखा जिसके अंतर्गत ताप तथा ऊष्मा की अभिधारणाओं एवं ऊष्मीय ऊर्जा का अन्य ऊर्जाओं में या अन्य ऊर्जाओं का ऊष्मीय ऊर्जा में रूपांतरण का अध्ययन ऊष्मा गतिकी क़हलाती है।
ताप (T), दाब (P), आयतन (V), एन्ट्रापी (S) आदि ऊष्मा गतिकी निर्देशांक होते है। और जब निकाय एक अवस्था से दूसरी अवस्था में जाता है तब वह कुछ नियमों का पालन करता है। इन्हे ऊष्मा गतिकी नियम कहते हैं।
कार्य तथा ऊष्मा की तुल्यता (Equivalence of WorkandHeat)
किसी निकाय के ताप में वृद्धि दो प्रकार से हो सकती है-
(i) निकाय को ऊष्मा देकर तथा
(ii) उस निकाय पर यांत्रिक कार्य करके।
जूल के नियमनानुसार उचित परिस्थितियों में किसी निकाय पर किया गया कार्य (W) व उत्पन्न ऊष्मा (H) परस्पर समानुपाती होते हैं।
\[W\propto H\]
\[W=JH\]
ऊष्मा का यांत्रिक तुल्यांक (J) = \[4.2\times {{10}^{7}}\] अर्ग/कैलोरी होता है। यह भौतिक राशि नहीं है।
आंतरिक ऊर्जा- किसी निकाय की वह संचित ऊर्जा जिसके द्वारा बाह्य ऊर्जा प्रदान किये बिना निकाय कार्य करने की क्षमता रखता है आंतरिक ऊर्जा (Internal Energy) कहलाती है।
आंतरिक ऊर्जा एक अवस्था चर होता है अर्थात निकाय की अवस्था निर्भर करता है पथ पर नहीं।
ऊष्मा इंजन एवं दक्षता
ऊष्मा इंजन ऊष्मागतिकी के द्वितीय नियम के केल्विन - प्लांक (प्रथम) कथन पर कार्य करता है।
ऐसी युक्ति जो ऊष्मा का यांत्रिक कार्य में अविरत रूप से स्थान्तरण करता है ऊष्मा इंजन कहलाता है। ऊष्मा इंजन में कार्यकारी पदार्थ तप्त वस्तु से ऊष्मा लेकर ऊष्मा के एक भाग को कार्य में परिवर्तित करता है और शेष ऊष्मा को एक शीतल वस्तु को देता है। परन्तु आज तक कोई भी ऐसा इंजन नहीं बना जो तप्त वस्तु से ली गयी संपूर्ण ऊष्मा को कार्य में बदल सके और शीतल वस्तु को कुछ भी ऊष्मा न दे। ऊष्मा इंजन के तीन मुख्य भाग होते हैं
1. ऊष्मा स्रोत (Heat Source)- ऊष्मा 'स्रोत से कार्य करने के लिए ऊष्मा ली जाती है।
2. कार्यकारी पदार्थ (Working Substance)- स्रोत से ऊष्मा ग्रहण करता है।
3. सिंक (Sink)- सिंक का ताप स्रोत के ताप से नीचा होता है।
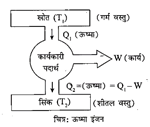
किसी ऊष्मा इंजन द्वारा एक चक्र में कार्यकारी पदार्थ प्रदान किये गये यांत्रिक कार्य W तथा एक चक्र में कार्यकारी पदार्थ द्वारा स्रोत से ली गयी ऊष्मा \[{{Q}_{1}}\] का अनुपात ऊष्मा इंजन की दक्षता कहलाता है।
कार्नो का ऊष्मीय इंजन (Carnot's Heat Engine)
सन 1824 में सांदी कार्नो नामक वैजानिक ने एक सैद्धांतिक इंजन की कल्पना की जिसके द्वारा उच्च ताप वाली वस्तु से.ग्रहण की गई ऊष्मा को पूर्णतः उपयोगी कार्य में परिवर्तन किया जाए तब ऐसे इंजन की दक्षता अधिक होगी। दो तापों के मध्य कार्य करने वाला कोई आदर्श उत्क्रमणीय ऊष्मा इंजन कार्नो इंजन कहलाता है।
कार्नो इंजन का कार्य \[\left( W \right)=\text{ }2.303R\left( {{T}_{1}}-\text{ }{{T}_{2}} \right)lo{{g}_{10}}\left( \frac{{{V}_{2}}}{{{V}_{1}}} \right)\]
कार्नो इंजन की दक्षता \[n=\left( 1-\frac{{{T}_{2}}}{{{T}_{1}}} \right)\]
इंजन की दक्षता 100% होने के लिए या तो सिंक का ताप 0 K या स्रोत का ताप \[\infty \]K होने चाहिए।
प्रशीतक या ऊष्मा पंप (Refrigerator or Heat Pump) ऊष्मा पंप, प्रशीतक के समान होता है। ये नाम युक्ति के प्रयोजन पर निर्भर करती है। यदि प्रयोजन किसी स्थान के कुछ भाग, जैसे की किसी प्रकोष्ठ के भीतरी भाग को ठंडा करता है, तो युक्ति को हम प्रशीतक कहते है। यदि प्रयोजन किसी स्थान के किसी भाग में ऊष्मा को पम्प करता है तो युक्ति को ऊष्मा पंप कहते हैं।
You need to login to perform this action.
You will be redirected in
3 sec
